西部首家大动物实验中心,西点科创推动国内外多款创新器械转化
导读:大动物实验是临床前研究的重要一环。随着国内创新器械不断发展、行业监管政策逐步完善,械企对临床前动物实验的需求将持续增长,这也对CRO企业的全生命周期服务能力提出了进一步的要求。
中国正在成为医疗器械创新的热土,相应的,CRO服务行业进入发展快车道。医疗器械CRO服务范围广泛,涵盖器械临床前的研发检测、动物实验;人体临床试验;注册申报;上市后生产体系法规及产品迭代研发的全生命周期服务。然而,多数CRO企业聚焦在临床试验及注册申报服务领域,国内临床前动物实验领域起步较晚,蓝海市场尚待开拓。
大动物实验是临床前研究的重要一环。随着国内创新器械不断发展、行业监管政策逐步完善,械企对临床前动物实验的需求将持续增长,这也对CRO企业的全生命周期服务能力提出了进一步的要求。4月,动脉网报道了国内领先的CRO企业,其中也谈到了科迈德打造的一站式器械转化平台,整合检测、临床前动物实验、临床试验服务。
早在2018年,科迈德团队便嗅到发展机遇,创办了西点科创(成都)生物科技有限公司(以下简称“西点科创”),2019年西部地区首家大动物实验中心正式运营。西点科创与四川大学国家生物医学材料工程技术研究中心张兴栋院士团队、华西医院团队紧密合作,可为医疗器械企业提供产品形式检测、临床前研究、临床研究、上市后培训/推广、国内外学术交流的一站式服务。
发展至今,西点科创已在结构性心脏病治疗器械大动物实验领域建立起领先地位,服务多家国内外知名械企,并不断加强在心血管及外周血管疾病治疗器械、卒中治疗器械、肺部疾病治疗器械等领域的服务优势,同时还在拓展有源器械、手术机器人等领域的大动物实验服务。
兽医学博士深耕临床前研究领域,做国内器械大动物实验的拓荒者
大动物实验是临床前研究的关键一环,可用于验证医疗器械的安全性及部分有效性,积累相关的实验数据,以推动企业及时调整产品设计、更高效地开展人体临床,大大降低临床试验受试者及术者的风险。如颅内取栓支架、人工心脏瓣膜、心脏起搏器、人工血管、止血粉等创新器械都需要做临床前大动物实验。
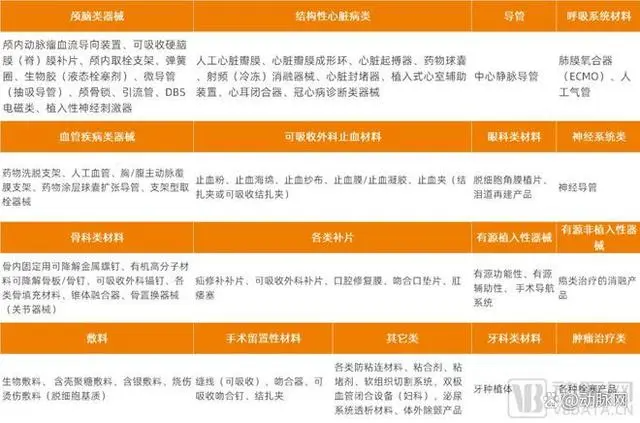
需开展动物实验的医疗器械
2019年前,医疗器械企业多集中在北上广地区,这些城市都有各自的大动物实验中心,而西南片区还处于空白。整体来看,国内大动物实验中心数量少且服务质量参差不齐,部分企业选择在医院或科研机构中开展动物实验,但这些机构缺乏相关人员和经验,可能在动物看护、数据收集等环节中出现问题。
大动物实验和人体临床的开展逻辑并不相同。临床前动物实验选取的都是健康的实验动物,无法做到完全符合人体,大动物实验的主要目的便是验证器械的安全性,包含一定有效性的内容,重点在于数据收集。而人体临床主要验证的是器械的有效性,重点放在对受试者疾病的改善上。
西点科创创始人贺伯德是兽医学博士出身,在临床前研究领域深耕30余年,相继担任过国际知名企业临床前科研负责人、参与创办管理多家大动物实验中心,已成功推动多个医疗器械产品的开发和审批,在结构性心脏病治疗器械、药物球囊、可降解冠脉支架等领域经验丰富。贺伯德博士拥有近30年的GLP动物实验经验,其过往参与的大动物实验经FDA审查均予以通过。
贺伯德博士非常重视大动物实验的规范性。他一直认为,动物实验所能看到的所有问题,在临床上都可能遇到。动物实验要做好临床前的最后一道门,让医生更安全地使用器械,对患者负责。正是这样的社会责任感,加上对中国蓝海市场的洞察,让他成为国内大动物实验领域“第一个吃螃蟹的人”,参与创办了国内首家大动物实验中心,并将其推向全国多个地区。
而也正是看到了西部地区大动物实验中心的空缺,贺伯德博士再次选择做“拓荒者”,创办了西点科创。以西点科创为新的出发点,他希望推动西部地区大动物实验的发展,赋能更多的创新械企,并以更高标准、更高质量的服务推动国内大动物实验领域发展。而凭借在中国医疗器械服务领域的突出贡献,贺伯德受到了业内及当地政府的高度赞赏。
实验中心遵循GLP原则,注重术后管理及动物福利
经过近几年的发展,我国创新医疗器械呈现爆发式增长,2022年期间便有67款三类医疗器械进入药监局创新审批绿色通道;国家层面出台《医疗器械动物试验研究注册审查指导原则》,进一步推动医疗器械临床前动物实验规范化;国内大动物实验中心数量稳步增长,部分械企、科研机构也在建设动物实验室。
医疗器械动物试验需符合3R(Replacement, Reduction and Refinement)原则和DQ(Design科学方案设计、Quality质量管理体系)原则,大动物实验中心的建设也并非易事。一家优秀的大动物实验中心应具备专业的技术团队、良好的临床前研究流程管理(实验动物筛选、异常动物留观处理、术后动物管理等)、先进的硬件设备(手术室功能齐备、高端影像设备等)、丰富的专家资源等。
同时,医疗器械领域GLP(良好实验室规范)认可是大势所趋。GLP可严格控制动物实验主客观因素,保证实验数据的质量和统一性、规范性、可靠性。
在美国、日本等地,医疗器械生物学评价均依照GLP规范进行管理,但在我国,医疗器械检测机构没有强制性要求按照GLP要求建设和组织。如在GLP体系内进行临床前评价,国内的实验数据有望获得国际认可,可推动我国医疗器械的国际化发展道路。
西点科创自成立起便按照AAALAC(国际实验动物管理评估与认证协会)标准设计建设,遵循GLP原则,致力于实现临床前大动物实验规范化、标准化。
人才团队是西点科创发展的基石,公司核心团队成员均在器械临床前研究领域深耕多年,且已有多年合作经验。
总经理在医疗器械领域从业近15年,熟悉临床前研究大动物实验中心建立的整套软硬件体系;临床前研究总监在医疗器械行业深耕超25年,开展过超3000例心血管器械植入术、肾动脉去神经术,擅长各种临床前研究的实验设计、预算编制、组织协调和报告撰写,且人员培训和管理经验丰富;技术专家从业近15年,开展过近1000例结构性心脏病器械动物实验,注重方案执行及术后动物管理。
在硬件层面,西点科创导管室、手术室搭建规范且配套齐全,配有飞利浦、奥林巴斯、GE等巨头的先进设备,导管室可开展介入手术培训,多功能培训手术室可同时开展8台外科手术。在资源层面,西点科创已与国内外多位专家学者建立合作,且拥有国际资源库,创始人贺伯德博士在美国便运营管理了3家GLP临床前动物实验中心,并与国外领先的大动物实验机构建立合作关系,共同助力器械转化。
在多方优势加持下,西点科创可提供产品形式检测、临床前研究、临床研究、上市后培训/推广、国内外学术交流的一站式服务。在核心的大动物实验中,公司尤其重视术后管理和动物福利,保持对实验动物的关怀和敬畏,规范化管控实验流程,致力于提供完整有效的动物实验数据。
同时,西点科创还可与科迈德、东点医学(全布局的三方公共服务平台,整合检测、临床前动物实验、临床试验)一同为器械客户提供全流程的器械转化服务,器械企业只需把在研产品给到他们,便不用操心接下来的检测、动物实验、人体临床、注册等一系列流程。在这过程中,三家企业也可实现资源共享、协同发展。
推动多款器械成功进入人体临床,实现国际化发展
自2019年正式运营以来,西点科创已在结构性心脏病治疗器械、卒中治疗器械、肺部疾病治疗器械、可降解血管支架、药物洗脱球囊等领域建立起优势地位,服务了多款国内首创器械产品。经公司测试的器械产品中,已有多款成功进入到临床试验阶段,并有3项研究通过国家重点研发计划项目。
同时,西点科创已建立起稳定的客户源,拥有多家长期合作企业,其中不乏海外巨头。公司不仅可帮助海外巨头在国内开展动物实验、推动器械转化,还可联合国外领先的大动物实验中心,助力国产创新器械在海外开展GLP动物实验,同时推动其临床实验的开展。
发展过程中,西点科创还与国家生物医学材料工程技术研究中心、四川省创新医疗器械临床研究院等达成战略合作。
在西点科创团队看来,随着国内创新器械发展,大动物实验中心数量还将持续增长。但大动物实验中心不仅是硬件配置的解决,还关系到团队的经验、对整体流程的把控等,行业发展还有待规范化。同时,价格战并不可取,降价可能破坏市场正常发展,并带来服务质量上的参差。
未来,西点科创将继续深耕临床前动物实验,进一步提高大动物实验的规范性,为全国的械企和科研院所提供优质服务,并通过交流合作推动全省、全国大动物实验实现规范化。同时,作为医疗器械一站式转化平台上的重要一环,在本月26日东点医学正式开业后,还将与科迈德、东点医学进一步协同发展,扎根国内多个省市,并实现全球化发展。