宜明昂科二次递表港交所:两年亏11亿,商业化前景仍不明朗
导读:继前次递表失效后,近日,宜明昂科生物医药技术(上海)股份有限公司(简称“宜明昂科”)再次向港交所递交IPO申请并获得受理。
继前次递表失效后,近日,宜明昂科生物医药技术(上海)股份有限公司(简称“宜明昂科”)再次向港交所递交IPO申请并获得受理。钛媒体App注意到,随着全球肿瘤免疫市场的迅速崛起,大量资本纷纷涌入这一前沿赛道。成立仅七年的宜明昂科先后完成6轮融资,估值达到8.3亿美元。
然而,创新药赛道本身属于高风险、长周期的行业,失败率极高。宜明昂科自成立以来持续烧钱投入研发,尽管有十余款药品同时在研,但目前为止尚未有一款产品实现商业化。研发投入能否带来相应的资本回报?对于宜明昂科来将,一切还是未知数。
两年亏11亿,尚未产生销售收入
招股书显示,宜明昂科成立于2015年,作为一家临床阶段生物技术公司,致力于开发创新肿瘤免疫疗法,是全球少数能够采用系统方法利用先天性免疫和适应性免疫系统治疗癌症的生物技术公司。
公司已开发出包含十多款创新候选药物的管线、8个正在进行的临床研究项目,围绕着固有免疫和获得性免疫多个潜力靶点布局了一系列产品,包括以CD47为靶点的融合蛋白和多款双抗,以及CD24、CD70等少见的靶点在研药物等。
根据弗若斯特沙利文的资料,在全球多个开发CD47靶向分子的药物研发企业中,宜明昂科是仅有的两家在单药治疗临床试验中观察到完全缓解(CR)并具有良好耐受安全性的公司之一。
宜明昂科目前尚无产品实现商业化,因此没有产生任何销售收入。据招股书显示,公司2021年及2022年分别确认收入506万元及53.8万元。收入来源为授权许可费、销售细胞株及其他產品以及提供检测服务。
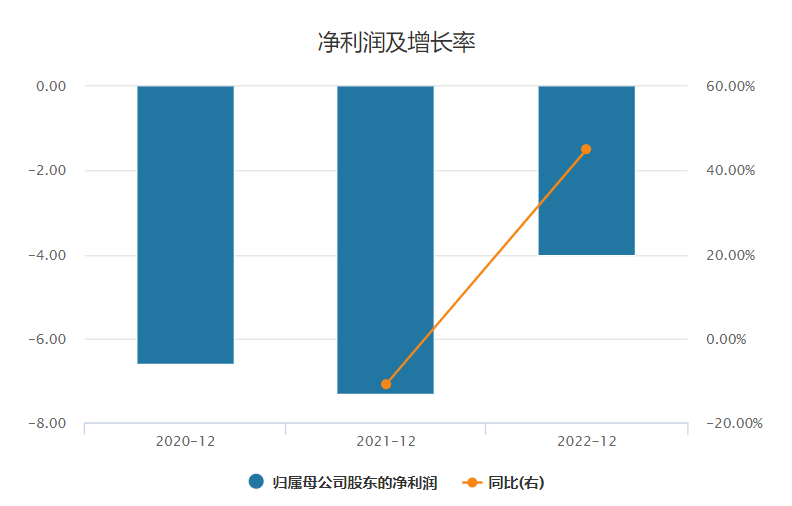
净利润情况,来源:Wind
报告期内,宜明昂科持续亏损,其中2021年及2022年,公司亏损分别为7.33亿元及4.03亿元,两年合计亏损11.36亿元。剔除公允值变动及按非国际财务报告准则计量的经调整亏损净额分别为1.83亿元及2.26亿元,亏损额度进一步扩大。
如果算上2020年亏损的6.6亿元,宜明昂科三年合计亏损了17.96亿元。宜明昂科预计,2023年的亏损净额将较2021年及2022年持续增加。
大量管线开发,需要源源不断的资金支持。成立至今,宜明昂科已获得多轮融资。公开信息显示,宜明昂科2015年6月成立时即获得30万美元的种子轮融资。自创立以来,宜明昂科获包括礼来、龙磐资本、张科领弋创投、洲岭资本、张江科投、阳光人寿、朗盛投资等在内十多家投资机构的投资,于2017年至2022年完成3000万元(单位人民币,下同)Pre-A轮、9000万元A轮、4000万元Pre-B轮、2.4亿元B轮、6500万美元B+轮以及8750万美元C轮融资。
截至2022年1月C轮融资完成后,宜明昂科估值8.3亿美元,折合港币约为65亿元。
研发开支过大,商业化前景不明
庞大的研发支出,是导致宜明昂科亏损的主要原因。招股书显示,公司研发开支由2021年的1.76亿元增加至2022年的2.77亿元。
安永大中华区生命科学与医疗健康行业联席主管合伙人吴晓颖对钛媒体App表示,创新药赛道本身属于高风险、长周期的行业,其核心竞争力就在于持续的研发能力。不过,对于临床阶段往商业化发展的企业,研发占比必定会从极高的比例慢慢走到相对合理的区间。
“成功的药企除了研发能力,还必须不断投资在企业的商业化能力,以及内部的运营管理能力。”吴晓颖认为,健康的财务表现才能做到自我输血,夯实管线的厚实度,反过来又提升企业的长期发展源动力。这是一个需要不断动态调整达到平衡的过程。
招股书显示,宜明昂科目前有十余款靶向先天性和适应性免疫系统的候选药物在研,包括5款处于临床阶段(已有7个正在进行的临床研究项目)、3款处于IND准备阶段和多款处于发现阶段及临床前阶段的候选药物。
从研发管线进度来看,上述核心产品均未进入关键性试验阶段,距离商业化还有一段距离。
公司的核心产品IMM01正是处于临床阶段的新一代CD47靶向分子,拟与其他药物联用治疗多种血液肿瘤(包括骨髓增生异常综合征(MDS)、急性髓系白血病(AML)、慢性粒-单核细胞白血病(CMML)及经典霍奇金淋巴瘤(cHL))和实体瘤(其中包括非小细胞肺癌(NSCLC)、小细胞肺癌(SCLC)、头颈部鳞状细胞癌(HNSCC)及结直肠癌(CRC))。
招股书显示,目前全球共有21个CD47靶向双特异性分子处于临床开发阶段,其中八个在中国进行临床试验。其中,IMM0306为国内首个进入I期临床试验的IgG1CD47×CD20双特异性抗体,在体外不与红细胞结合。此外,IMM2902是全球唯一一个进入临床阶段的CD47×HER2双特异性分子。
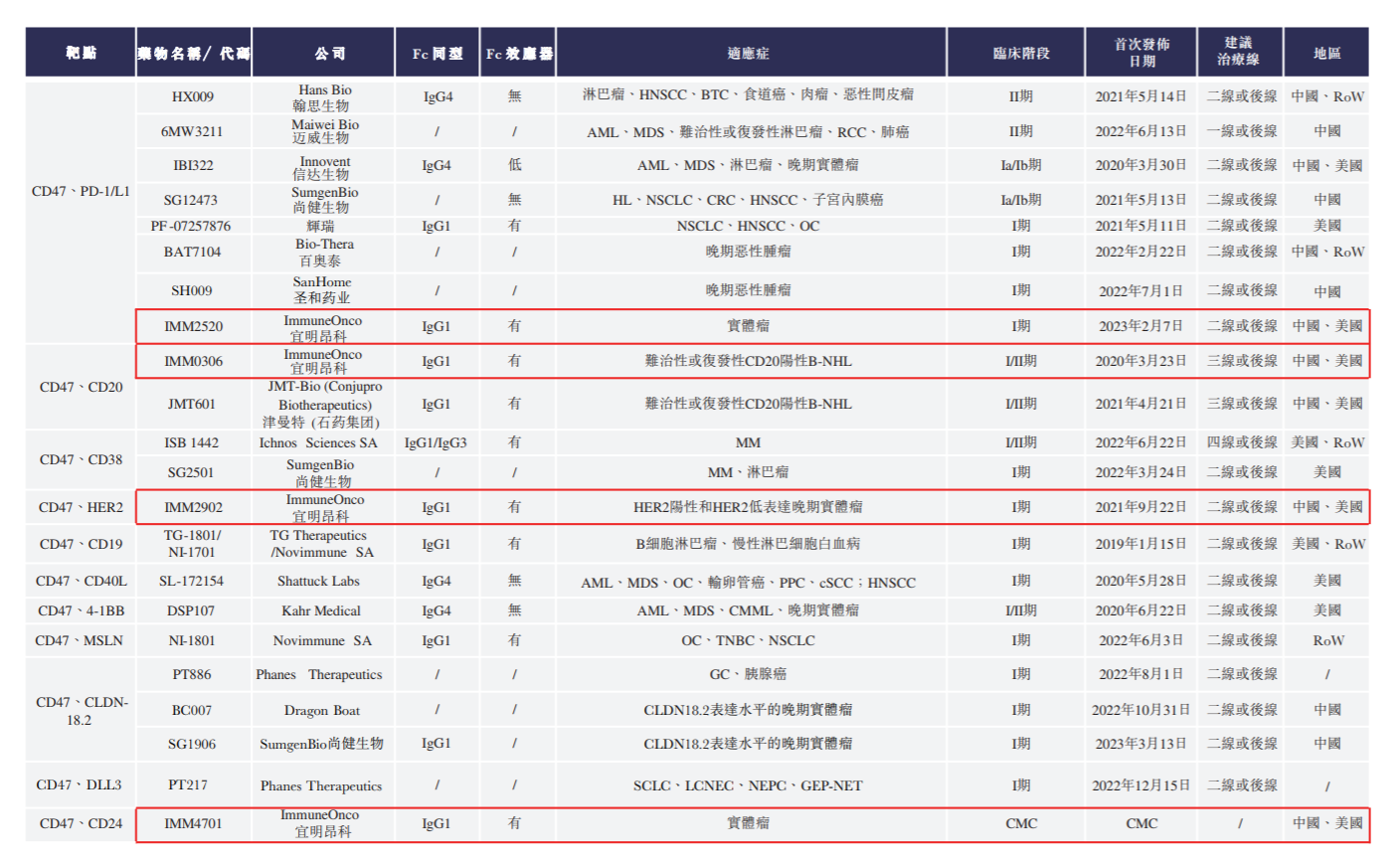
CD47靶向双特异性分子全球管线,来源:招股书
值得注意的是,设计及开发有效而安全的CD47靶向药物需要一定的门槛,尤其是在安全性上。此前多个CD47抗体的临床试验已因安全问题暂停或部分暂停,例如BMS(新基)的CC-90002、Surface Oncology的SRF231。
尽管安全性一直是有关靶向CD47的药物,尤其是CD47抗体的首要问题,但在临床试验中仍难以避免不良反应的发生。就CD47抗体而言,其与人体红细胞和血小板(普遍表达CD47)会有不可避免的结合,进而可能导致严重的血液毒性,如贫血、血小板减少症和血凝反应。
与此同时,肿瘤赛道选手云集。在中国及全球范围内,目前有52种CD47/SIRPα靶向候选药物正处于临床开发阶段,包括融合蛋白、单克隆抗体及双特异性分子,由中国的23家药物开发商及中国以外全球的22家药物开发商开发。
研发扎推或导致产品同质化,随著新药陆续获批进入市场,宜明昂科所面临的竞争压力不容小觑。
作者 | 马琼