研究:随着阿尔茨海默病的发展,大脑中调节DNA折叠的酶的水平出现下降
导读:来自匹兹堡大学、麦吉尔大学和哈佛大学的研究人员发现,与早期的研究相反,随着阿尔茨海默病的恶化,大脑中控制DNA折叠的酶的水平发生下降。
来自匹兹堡大学、麦吉尔大学和哈佛大学的研究人员发现,与早期的研究相反,随着阿尔茨海默病的恶化,大脑中控制DNA折叠的酶的水平发生下降。他们的研究结果于最近发表在《Nature Communications》上。
这些挑战教条的发现显示,组蛋白去乙酰化酶I(HDAC I)水平的下降是控制DNA如何在细胞核内包装的酶之一,这跟折叠错误的β-淀粉样蛋白和tau蛋白的负面影响及阿尔茨海默病相关的认知能力下降有关。这些结果在两个独立的阿尔茨海默病活体患者队列及死后脑组织上得到了验证。
重要的是,新发现意味着使用HDAC抑制剂--减少HDAC水平的药物,目前正在对轻度阿尔茨海默病进行临床试验--可能会对患者造成伤害而不是受益。
这项研究的论文第一作者Tharick Pascoal医学博士说道:“约三分之一有脑淀粉样病变的老人不会发展成阿尔茨海默病。现在我们有证据表明另一个决定疾病是否会进一步发展的因素,它跟大脑环境如何影响我们基因的表达有关。”据悉,Pascoal还是皮特大学医学院精神病学和神经学的助理教授。
阿尔茨海默病是一种致命的神经退行性疾病,通常影响的对象是老年人,但这种疾病在症状出现前几十年就开始了。有4400万人患有阿尔茨海默病或相关的痴呆症。阿尔茨海默病患者随着时间的推移出现认知障碍,包括记忆力下降和思考及说话困难,这是由于错误折叠的β-淀粉样蛋白和纠缠的tau蛋白链形成斑块进而诱发神经细胞死亡和脑组织损伤造成。
然而淀粉样蛋白和tau蛋白紊乱只是复杂画面中的一个部分。在过去的几十年时间里,研究人员已经开始关注其他过程-神经炎症和脑细胞化学环境的变化及这些过程如何影响病情的发展。
其中一个过程被称为表观遗传组蛋白修饰。细胞可以通过修改DNA在细胞核内的折叠方式来调整遗传信息转化为新蛋白质模板的效率--无论它是紧紧包裹在称为组蛋白的蛋白质桶上还是挂在较松散的线上。这使细胞能迅速和可逆地修改我们的基因运作方式并对环境的变化作出反应而去不改变DNA序列本身。
在长期寻求开发安全、有效的疗法以避免认知能力下降和扭转疾病进展的过程中,一种驱动表观遗传修饰的亚型酶-HDACs-成为新的阿尔茨海默病疗法的前景目标。
HDACs通过进行一种化学反应以鼓励将DNA分子更紧密地包装成凝聚的束并限制新蛋白质的生物合成以应对环境线索。
早期对死后大脑样本的研究报告称,随着疾病的发展,阿尔茨海默病患者大脑中的HDACs水平会增加。高水平的HDACs被认为限制了大脑产生新的功能性蛋白质的能力,这些蛋白质构成了关键的细胞成分,因此导致了记忆丧失和认知能力下降。
然而这篇新论文挑战了现状并为已经混乱的局面增加了另一块。HDAC I的丧失可能跟β-淀粉样蛋白和tau病症的出现有机理上的联系--正如Pascoal及其同事在上一篇论文中所显示的那样,这些病症跟脑组织炎症交织在一起并推动阿尔茨海默病的发展--而且在伴随该疾病的认知变化之前。
为了确保研究结果代表了不同患者群体的真实情况,研究人员在加拿大麦吉尔大学和马萨诸塞州综合医院进行了两项平行但完全独立的研究,他们总共招募了94名参与者。这两个地方在整个研究期间没有交流且在不知道另一组研究结果的情况下提交了他们的结果。
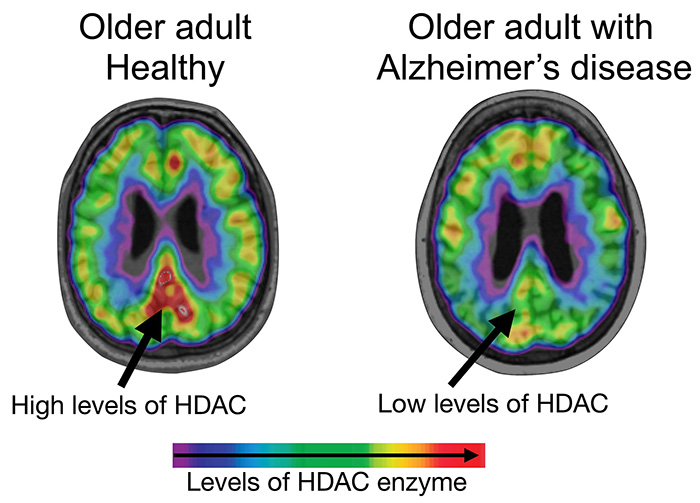
研究人员使用一种名为(11C)Martinostat的选择性分子示踪剂显示,跟非阿尔茨海默病对照组相比,阿尔茨海默病患者大脑中的HDAC I水平大大降低,尤其是在埋藏在大脑核心深处的区域--海马体和中线--及大脑的颞叶皮质。
分析显示,在最容易受到阿尔茨海默病相关退行性变化影响的大脑区域,HDAC I的减少跟较高的β-淀粉样蛋白和tau负担相对应。另外它还预测了两年内进行性的神经变性和认知能力下降。
虽然研究人员相信,管理临床试验设计的严格程序确保了病人安全的最高标准,但他们警告称,测试HDAC抑制剂的努力可能是错误的。他们指出,相反,该领域需要进一步探索HDAC激活和疾病进展之间的关系并确定在总共18种HDAC中哪一类在阿尔茨海默病相关的大脑病理中起着关键作用。
不过,科学家们还是非常乐观。
“好消息是,从本质上讲,表观遗传过程是可以改变的。未来的治疗方法有很大的希望,另外将抗淀粉样蛋白疗法跟能挽救HDACs损失的药物结合起来有着很大的希望,”Pascocal说道。